高效准确预测DDI,福大、元星智药团队解释性药物AI模型,登Nature子刊
来源:机器之心
时间:2024-09-06 17:55:08 358浏览 收藏
一分耕耘,一分收获!既然都打开这篇《高效准确预测DDI,福大、元星智药团队解释性药物AI模型,登Nature子刊》,就坚持看下去,学下去吧!本文主要会给大家讲到等等知识点,如果大家对本文有好的建议或者看到有不足之处,非常欢迎大家积极提出!在后续文章我会继续更新科技周边相关的内容,希望对大家都有所帮助!

意外的药物相互作用 (DDI) 是药物研究和临床应用的重要问题,因为其极有可能引发严重的药物不良反应或药物停药。
虽然许多深度学习模型在 DDI 预测方面取得了很好的成果,但模型可解释性以揭示 DDI 的根本原因尚未得到广泛探索。
福州大学、福建医科大学第一附属医院以及元星智药的研究人员提出 MeTDDI——一种深度学习框架,具有局部-全局自注意力和共同注意力,用于学习基于主题的 DDI 预测图。
关于可解释性,研究人员对 73 种药物(13,786 个 DDI)进行了广泛的评估,MeTDDI 可以精确解释涉及 58 种药物的 5,602 个 DDI 的结构机制。此外,MeTDDI 显示出解释复杂 DDI 机制和降低 DDI 风险的潜力。
MeTDDI 为探索 DDI 机制提供了一个新的视角,这将有利于药物发现和多重用药,从而为患者提供更安全的治疗。
该研究以「Learning motif-based graphs for drug–drug interaction prediction via local–global self-attention」为题,于 2024 年 8 月 27 日发布在《Nature Machine Intelligence》。

由于老龄化和多重疾病,药物组合或多重用药被广泛使用,并可能对公共卫生和经济造成影响。尽管多重用药具有治疗效果,但存在发生意外药物间相互作用 (DDI) 的风险,这可能导致严重的药物不良反应 (ADR) 甚至停药。
因此,提前预测 DDI 将会对药物研究和临床环境带来巨大好处,从而提高药物安全性并保护患者健康。通过体外和体内实验进行 DDI 评估很有用,但成本高、耗时且费力,阻碍了大规模 DDI 筛选的实用性。
如今,深度学习模型已成为高通量准确 DDI 预测以及根本原因解释的有前途的替代方案。
在最新的研究中,福州大学、福建医科大学第一附属医院以及元星智药的研究团队重点关注代谢介导的药物相互作用(MMDDI)的预测,并提出了基于分子结构的深度学习框架 MeTDDI,用于预测 MMDDI。
该方法主要用于解决 DDI 预测中的三个挑战:(1) 学习分子内和分子间亚结构相互作用,(2) 预测 DDI 相关的药物代谢,(3) 广泛提供和评估模型的可解释性。
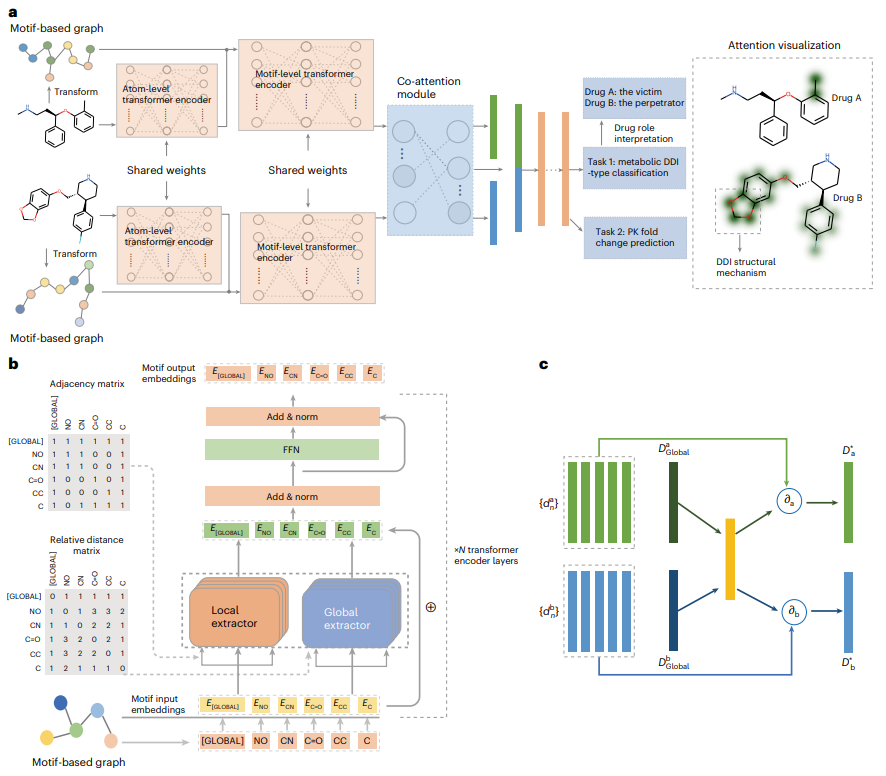
受益于局部-全局自注意力和共同注意力结构,MeTDDI 可以有效地学习基于基序的图内/图之间的分子内和分子间子结构相互作用,从而进行 DDI 推理。
评估结果表明,它在分类和回归任务中都取得了与基线相比具有竞争力的性能。MeTDDI 还可以准确识别药物(perpetrator 或 victim)在 DDI 中的机制作用,并量化 perpetrator 对 victim PK 的影响,这对药物研究和临床应用都非常有益。
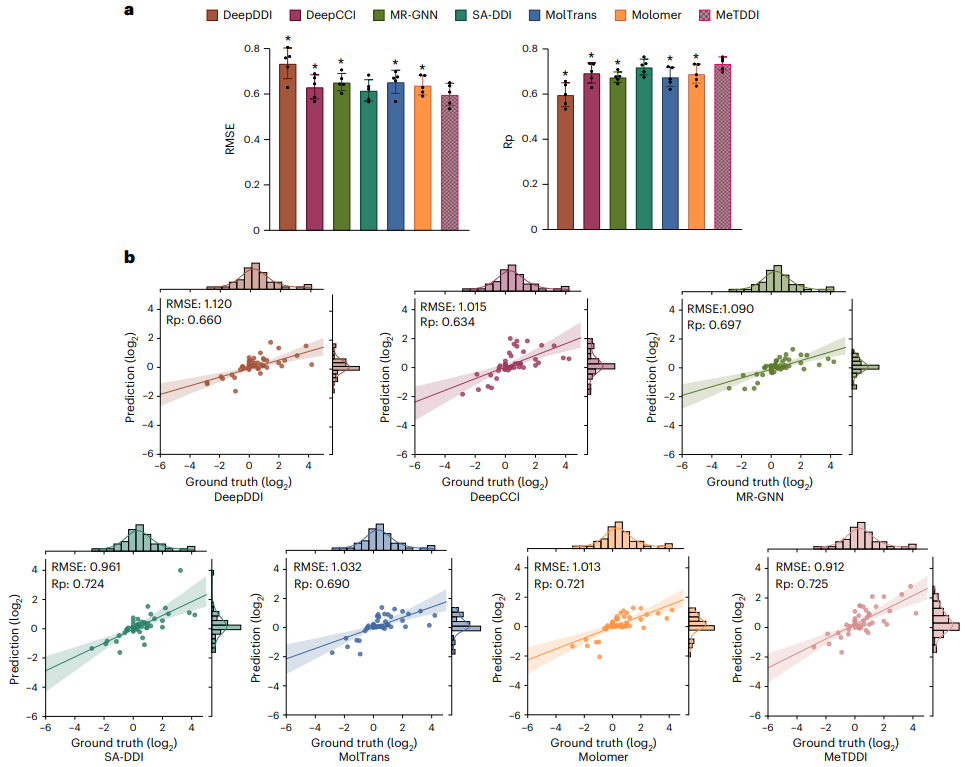
关于模型的可解释性,MeTDDI 展示了识别与 DDI 相关的关键机制子结构的能力。
首先,MeTDDI 可视化的关键子结构与文献中对 73 种代表性化合物(具有 13,786 个 DDI 对)的分析中报道的关键子结构大致匹配。
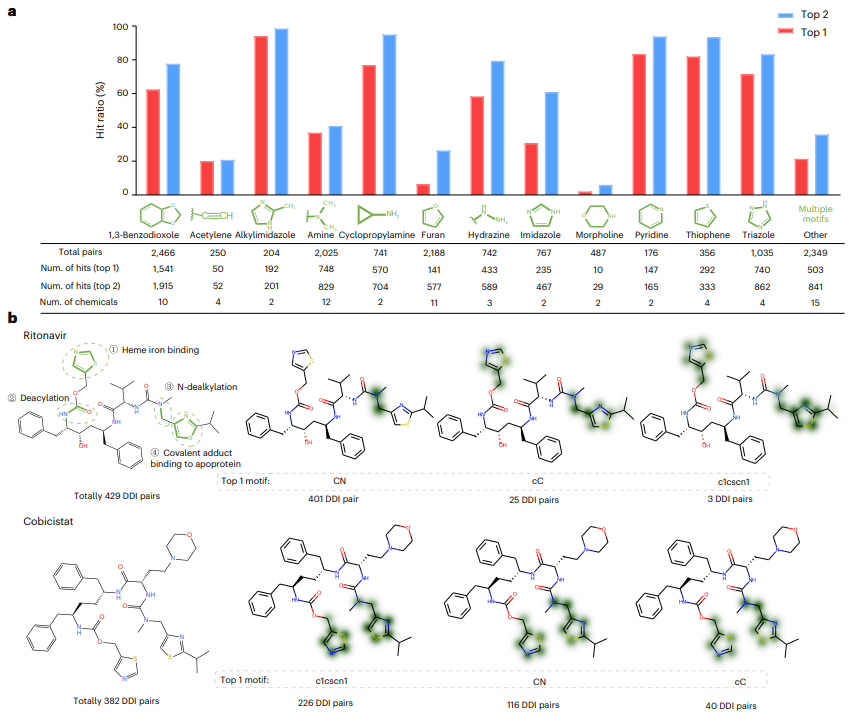
其次,研究人员评估了 MeTDDI 以及两个最先进的模型(即 CIGIN 和 CGIB)的模型可解释性。结果表明,MeTDDI 在模型可解释性方面也表现出优异的性能。
此外,MeTDDI 可以突出显示与酶抑制相关的化学物质的代谢位点。
MeTDDI 的优势
传统方法仅仅通过体外测试 perpetrator 的代谢酶抑制来解释 DDI 机制,而没有充分考虑 victim。这是有问题的,因为 perpetrator 对酶抑制的效力可以根据 victim 的化学特性而改变。
Victim可能会改变 perpetrator 与代谢酶(尤其是 CYP)的结合或相互作用模式,从而导致各种酶抑制机制。这也许可以解释为什么一些化学物质(如炔雌醇和孕二烯酮)在体外单独使用时是代谢酶的强效抑制剂,但与其victim结合时效力就会降低。这也许可以解释为什么研究中只观察到乙炔雌二醇的两次反应,这被视为体外灭活 CYP3A4 的机制。
此外,帕罗西汀和伊曲康唑的案例研究表明,MeTDDI 正确地预测了化学物质中的基序变化并与生物实验的结果相匹配,表明其有潜力帮助研究人员修改药物结构以减轻 MMDDI 风险。
总而言之,MeTDDI 增强了 DDI 预测能力,为理解和探索 DDI 机制提供了新的视角,这将有利于药物研发和多重用药,从而为患者提供更安全的治疗。
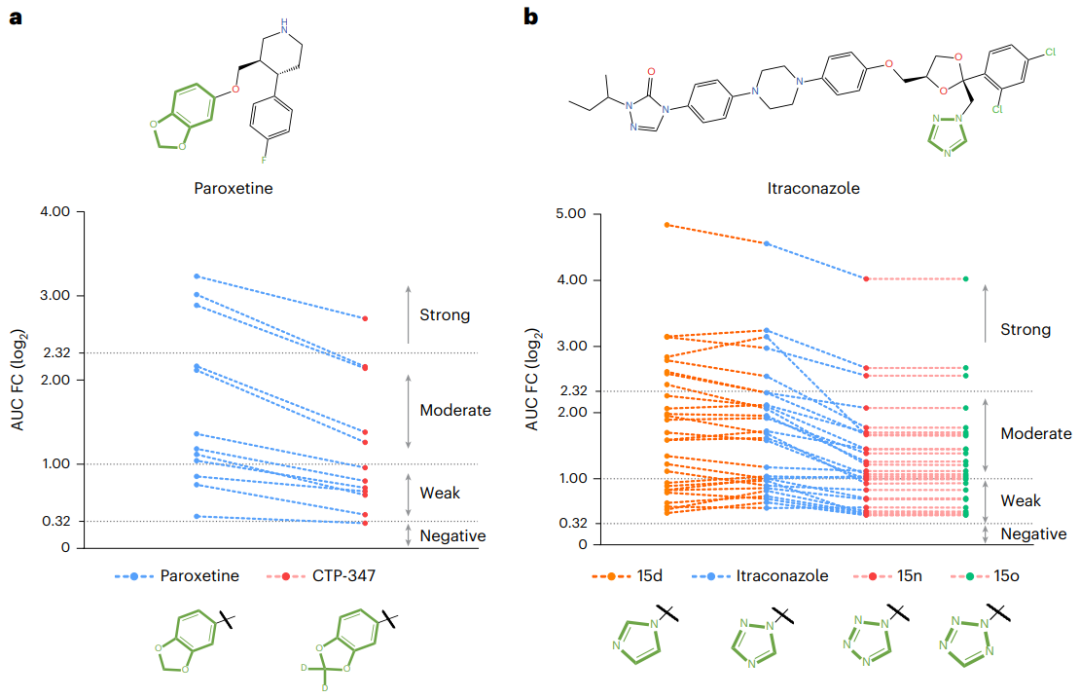
图示:两个使用 MeTDDI 缓解 DDI 的案例研究。(来源:论文)MeTDDI 的改进方向
MeTDDI 具有诸多优势,同时,它也存在一些局限性。
首先,在困难场景中,准确预测具有挑战性。这可能源于 DDI 机制的多样性和复杂性以及仅依赖药物结构的局限性。
由于 MMDDI 需要两种药物在相同的代谢酶上相互作用,因此可以将酶特征纳入模型中,以便更好地学习。然而,一些代谢酶(如 CYP)表现出药物-酶相互作用位点的非凡灵活性;因此,酶特征的建模仍然是一个挑战。
其次,MeTDDI 训练的数据集基于 FDA 药品标签,这是对人群的统计观察,可能无法反映个别患者的特征。因此,在可用的情况下,应考虑个别患者的数据,以便将来开发模型并做出更精确的预测。第三,MeTDDI 可能难以同时预测两种以上药物的相互作用。
然而,确保多重用药安全的一般做法是搜索所有可能的药物对之间的成对 DDI;可以通过枚举所有药物对来直接部署 MeTDDI 来预测多种药物之间的 DDI。
最后,对于 DDI 基础的全新发现的子结构,可以采用分子对接等替代技术作为补充方法来增强 MeTDDI 可视化功能的可信度。并且,研究人员表示,分子对接是 MeTDDI 的宝贵补充工具。
论文链接:https://www.nature.com/articles/s42256-024-00888-6
今天关于《高效准确预测DDI,福大、元星智药团队解释性药物AI模型,登Nature子刊》的内容就介绍到这里了,是不是学起来一目了然!想要了解更多关于理论的内容请关注golang学习网公众号!
-
501 收藏
-
501 收藏
-
501 收藏
-
501 收藏
-
501 收藏
-
345 收藏
-
211 收藏
-
497 收藏
-
396 收藏
-
350 收藏
-
122 收藏
-
426 收藏
-
257 收藏
-
375 收藏
-
313 收藏
-
480 收藏
-
414 收藏
-

- 前端进阶之JavaScript设计模式
- 设计模式是开发人员在软件开发过程中面临一般问题时的解决方案,代表了最佳的实践。本课程的主打内容包括JS常见设计模式以及具体应用场景,打造一站式知识长龙服务,适合有JS基础的同学学习。
- 立即学习 543次学习
-

- GO语言核心编程课程
- 本课程采用真实案例,全面具体可落地,从理论到实践,一步一步将GO核心编程技术、编程思想、底层实现融会贯通,使学习者贴近时代脉搏,做IT互联网时代的弄潮儿。
- 立即学习 516次学习
-

- 简单聊聊mysql8与网络通信
- 如有问题加微信:Le-studyg;在课程中,我们将首先介绍MySQL8的新特性,包括性能优化、安全增强、新数据类型等,帮助学生快速熟悉MySQL8的最新功能。接着,我们将深入解析MySQL的网络通信机制,包括协议、连接管理、数据传输等,让
- 立即学习 500次学习
-

- JavaScript正则表达式基础与实战
- 在任何一门编程语言中,正则表达式,都是一项重要的知识,它提供了高效的字符串匹配与捕获机制,可以极大的简化程序设计。
- 立即学习 487次学习
-

- 从零制作响应式网站—Grid布局
- 本系列教程将展示从零制作一个假想的网络科技公司官网,分为导航,轮播,关于我们,成功案例,服务流程,团队介绍,数据部分,公司动态,底部信息等内容区块。网站整体采用CSSGrid布局,支持响应式,有流畅过渡和展现动画。
- 立即学习 485次学习

